Research (English here)
ナノとバイオの融合領域の研究を行っています。特に、ナノマテリアル(金属ナノ粒子・カーボンナノチューブなど)とナノ・マイクロチップ技術を駆使し、遺伝子、抗体、細胞など優れたバイオの機能を活用したバイオセンサー、細胞デバイス、一分子アッセイ、バイオマス変換システムなど革新的技術の開拓に取り組んでいます。(1)ナノフォトニックバイオデバイスに関する研究
局在表面プラズモン共鳴と薄膜干渉を利用した新規フォトニックバイオセンサー
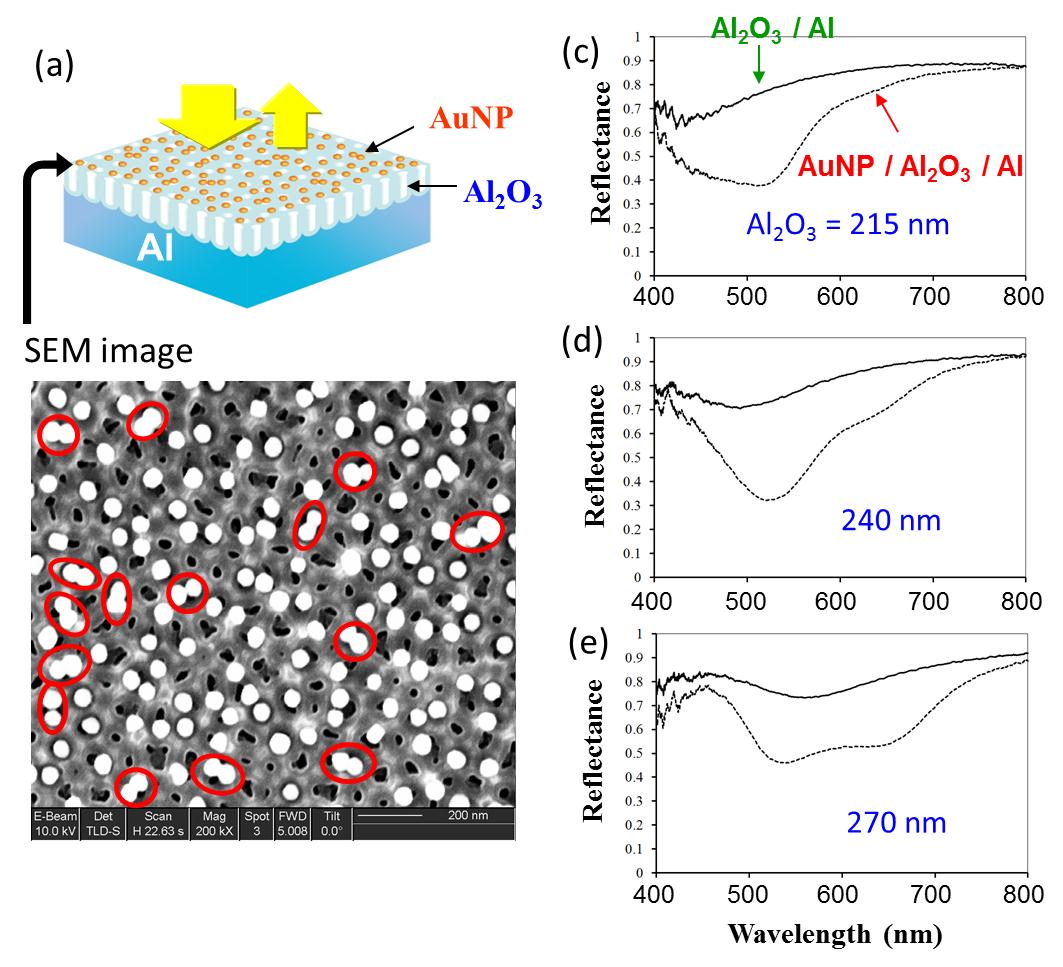 誘電体透明薄膜を金ナノ粒子層と金属または半導体基板で挟んだ多層膜構造を設計し、局在表面プラズモン共鳴(LSPR)の変化を薄膜干渉に基づく反射スペクトル中のフリンジパターンの変化として捉える新規LSPRバイオセンサーを開発している。一般的なLSPRセンサーの感度は金属ナノ粒子のサイズ、形状、配列構造に依存するが、本センサーでは薄膜構造を制御することによって単にスペクトル形状が変化するというだけでなく、特定のプラズモンバンドを選択的に励起できることができる。実際にポーラスアルミナ表面に金ナノ粒子を固定化することにより形成される金ナノ粒子二量体のLSPRを選択的に励起する構造を作製し、感度や光電場の増強を実験・理論の両面から解明している。
誘電体透明薄膜を金ナノ粒子層と金属または半導体基板で挟んだ多層膜構造を設計し、局在表面プラズモン共鳴(LSPR)の変化を薄膜干渉に基づく反射スペクトル中のフリンジパターンの変化として捉える新規LSPRバイオセンサーを開発している。一般的なLSPRセンサーの感度は金属ナノ粒子のサイズ、形状、配列構造に依存するが、本センサーでは薄膜構造を制御することによって単にスペクトル形状が変化するというだけでなく、特定のプラズモンバンドを選択的に励起できることができる。実際にポーラスアルミナ表面に金ナノ粒子を固定化することにより形成される金ナノ粒子二量体のLSPRを選択的に励起する構造を作製し、感度や光電場の増強を実験・理論の両面から解明している。
References: 1)H. Minh Hiep, H. Yoshikawa, M. Saito, E. Tamiya, ACS Nano, Vol.3, 446-452 (2009), 2) H. Minh Hiep, H. Yoshikawa, E. Tamiya, Analytical Chemistry, Vol.82, 1221-1227 (2010), 3) H. Minh Hiep, H. Yoshikawa, E. Tamiya et al., Japanese Journal of Applied Physics, Vol.49, 06GM02 (2010)
ナノインプリント技術を利用した新規LSPRバイオセンサーチップの開発
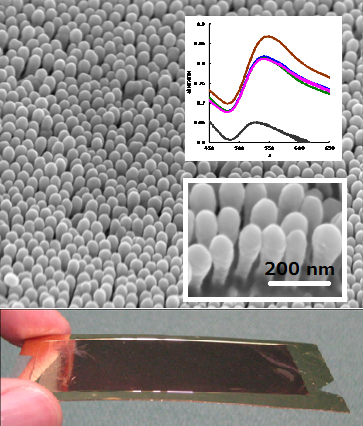 ナノインプリント技術による微細加工技術は、ナノ構造を大面積、大量かつ再現性よく作製することが期待できる。この特徴を活かた金ナノ構造を有するプラズモンチップの開発にも取り組んでいる。ナノ細孔を有するポーラスアルミナを鋳型として用いて、熱ナノインプリントを行い、フィルム樹脂にナノ突起構造を形成した。スパッタリングにより金を堆積させ、光学特性を付与したところ、600 nm付近に吸収ピークが観測され、また屈折率の異なる媒質に応じた吸収ピークシフトが見られた。抗原抗体反応モデルとして、IgG計測を行い、10ng/mLの感度を達成しており、現在、バイオチップ応用や高感度・高機能化へ向けた取り組みを進めている。
ナノインプリント技術による微細加工技術は、ナノ構造を大面積、大量かつ再現性よく作製することが期待できる。この特徴を活かた金ナノ構造を有するプラズモンチップの開発にも取り組んでいる。ナノ細孔を有するポーラスアルミナを鋳型として用いて、熱ナノインプリントを行い、フィルム樹脂にナノ突起構造を形成した。スパッタリングにより金を堆積させ、光学特性を付与したところ、600 nm付近に吸収ピークが観測され、また屈折率の異なる媒質に応じた吸収ピークシフトが見られた。抗原抗体反応モデルとして、IgG計測を行い、10ng/mLの感度を達成しており、現在、バイオチップ応用や高感度・高機能化へ向けた取り組みを進めている。
集光レーザー光を利用したナノバイオ解析
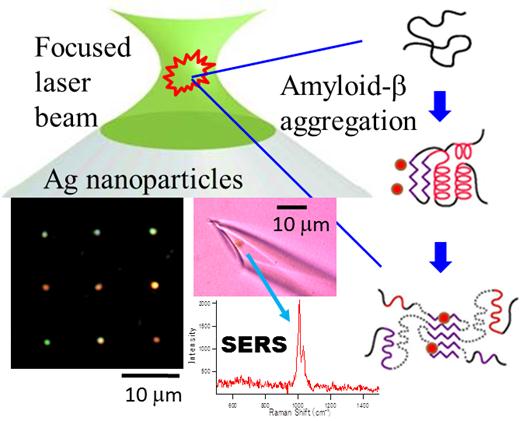 集光レーザー場における光化学反応や光放射圧などのレーザー誘起現象を利用した新しいバイオ分析技術の開発を進めている。1) アルツハイマー病との関連が注目されるアミロイド分子の初期凝集過程を、近赤外レーザーによる光トラップ下での二光子励起蛍光分光法により解析することに成功した。2)波長532nmのグリーンレーザーを利用して、明瞭なプラズモンバンドと表面増強ラマン散乱(Surface enhanced Raman scattering: SERS)活性を有する銀ナノ構造を作製することに成功した。本手法を活用し、インジェクション用のマイクロピペットの先端内部に銀ナノ粒子集合体を形成させ、内部に吸引した極微量試料のSERSスペクトル測定にも成功した。
集光レーザー場における光化学反応や光放射圧などのレーザー誘起現象を利用した新しいバイオ分析技術の開発を進めている。1) アルツハイマー病との関連が注目されるアミロイド分子の初期凝集過程を、近赤外レーザーによる光トラップ下での二光子励起蛍光分光法により解析することに成功した。2)波長532nmのグリーンレーザーを利用して、明瞭なプラズモンバンドと表面増強ラマン散乱(Surface enhanced Raman scattering: SERS)活性を有する銀ナノ構造を作製することに成功した。本手法を活用し、インジェクション用のマイクロピペットの先端内部に銀ナノ粒子集合体を形成させ、内部に吸引した極微量試料のSERSスペクトル測定にも成功した。
Reference: A. J. Veloso, H. Yoshikawa, X. R. Cheng, E. Tamiya, K. Kerman, Analyst 136, 4164 (2011)
(2)マイクロ流体バイオデバイスに関する研究
マイクロフルイディクス型迅速PCRチップの開発と検査応用
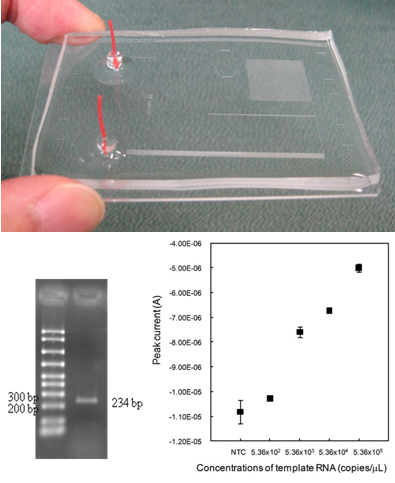 RNAウィルスの簡易迅速検知を目指し、マイクロフロー型RT-PCRデバイスの設計・作製に取り組んでいる。フローチップはRNAの逆転写反応にかかる領域(180 mm)、初期変性部(90 mm)、PCRサイクル部(930 mm、30cycles)、Pressurizing-channel (80mm)、計1280 mm(体積3.08μL)から構成される。新型インフルエンザを測定対象とし、作製したデバイスを用いたオンチップ遺伝子増幅を行ったところ、9.5分で目的のDNAを増幅することに成功した。また初期濃度53.6 copy/μLの新型インフルエンザウィルスからの検出にも成功した。現在、新たな迅速簡易増幅を可能とする集積チップ開発に取り組んでいる。
RNAウィルスの簡易迅速検知を目指し、マイクロフロー型RT-PCRデバイスの設計・作製に取り組んでいる。フローチップはRNAの逆転写反応にかかる領域(180 mm)、初期変性部(90 mm)、PCRサイクル部(930 mm、30cycles)、Pressurizing-channel (80mm)、計1280 mm(体積3.08μL)から構成される。新型インフルエンザを測定対象とし、作製したデバイスを用いたオンチップ遺伝子増幅を行ったところ、9.5分で目的のDNAを増幅することに成功した。また初期濃度53.6 copy/μLの新型インフルエンザウィルスからの検出にも成功した。現在、新たな迅速簡易増幅を可能とする集積チップ開発に取り組んでいる。
References: 1) Rapid detection for primary screening of influenza A virus: microfluidic RT-PCR chip and electrochemical DNA sensor, Keiichiro Yamanaka, Masato Saito, Kenji Kondoh, Mohammad Mosharraf Hossain, Ritsuko Koketsu, Tadahiro Sasaki, Naoki Nagatani, Kazuyoshi Ikuta and Eiichi Tamiya, Analyst, 2011, 136, 2064?2068, 2) An optimal design method for preventing air bubbles in high-temperature microfluidic devices, Tsuyoshi Nakayama, Ha Minh Hiep, Satoshi Furui, Yuji Yonezawa, Masato Saito, Yuzuru Takamura, Eiichi Tamiya, Anal Bioanal Chem, 396(1), 457-464, 2010
一細胞分離および解析のためのマイクロ流体デバイスの開発と応用
 再生医療において、安全性が高く(細胞の損傷が無い、目的外の細胞が含まれない等)、相当量の細胞数を準備可能なデバイスが必要となる。つまり、一細胞ごとの評価による目的とする細胞の選択、回収を、ハイスループットに行える技術が必要である。そこで、一細胞分離、評価が可能で、且つ、目的の細胞を回収することが可能なマイクロ流体デバイスの作製を目指している。 直径10μmの半円状のトラップサイトを設け、その先が3μmの流路となるパターンを設計し、フォトリソグラフィ技術に基づいて流路チップを作製した。流路内での細胞の吸着を防止するためのコーティング剤の検討などを進め、Jurkat細胞1個を捕捉、リリースを行えることを確認した。現在、流路の集積化に取り組んでおり、今後、実試料を用いた評価に取り組む予定である。
再生医療において、安全性が高く(細胞の損傷が無い、目的外の細胞が含まれない等)、相当量の細胞数を準備可能なデバイスが必要となる。つまり、一細胞ごとの評価による目的とする細胞の選択、回収を、ハイスループットに行える技術が必要である。そこで、一細胞分離、評価が可能で、且つ、目的の細胞を回収することが可能なマイクロ流体デバイスの作製を目指している。 直径10μmの半円状のトラップサイトを設け、その先が3μmの流路となるパターンを設計し、フォトリソグラフィ技術に基づいて流路チップを作製した。流路内での細胞の吸着を防止するためのコーティング剤の検討などを進め、Jurkat細胞1個を捕捉、リリースを行えることを確認した。現在、流路の集積化に取り組んでおり、今後、実試料を用いた評価に取り組む予定である。
(3)ES細胞分化の機能評価システムに関する研究
心筋細胞拍動イメージングと薬理
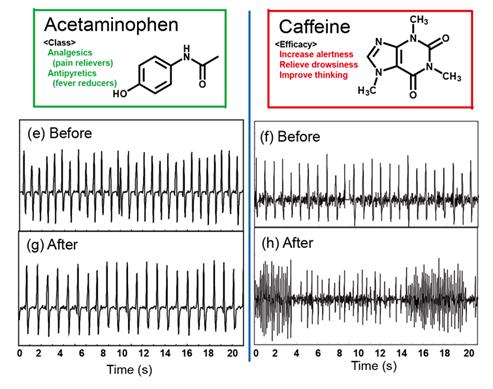 心筋細胞は実験室内における細胞培養環境下においても自律的に拍動する細胞である。拍動は本来の心臓の機能、特に拍動周期や拍動強度の動的機能をそのまま再現することが可能であり、心臓の機能不全や病態の解明、毒物の検査や診断など幅広い研究に用いられている。民谷研究室では、心筋細胞の拍動を非侵襲で測定することにより、心筋毒物試験にいける非侵襲測定方法を開発している。開発した非侵襲測定方法は顕微鏡画像の解析アルゴリズムによる微分画像分析によって、心筋の拍動周期および、伸縮運動量を定量できるものである。さらに、微分画像分析は従来の電極法によるものと同時測定を可能とする方法である。(図はアセトアミノフェンとカフェイをES細胞から分化させた心筋細胞に投与した際の心筋拍動jの微分画像分析による定量結果である。)
心筋細胞は実験室内における細胞培養環境下においても自律的に拍動する細胞である。拍動は本来の心臓の機能、特に拍動周期や拍動強度の動的機能をそのまま再現することが可能であり、心臓の機能不全や病態の解明、毒物の検査や診断など幅広い研究に用いられている。民谷研究室では、心筋細胞の拍動を非侵襲で測定することにより、心筋毒物試験にいける非侵襲測定方法を開発している。開発した非侵襲測定方法は顕微鏡画像の解析アルゴリズムによる微分画像分析によって、心筋の拍動周期および、伸縮運動量を定量できるものである。さらに、微分画像分析は従来の電極法によるものと同時測定を可能とする方法である。(図はアセトアミノフェンとカフェイをES細胞から分化させた心筋細胞に投与した際の心筋拍動jの微分画像分析による定量結果である。)
Reference: 1) Mohannad Mosharaf Hossain, Eiichi Shimizu, Sathuluri Ramachandra Rao,Masato Saito, Yoshinori Yamaguchi, Eiichi Tamiya, "Non-invasive characterization of Mouse Embryonic Stem cell derived Cardiomyocytes based on the intensity variation in digital beating video", Analyst, 2010,135, 1624-1630 (2010)
EmbryonicStem(ES)細胞分化の非侵襲ラマン分光解析
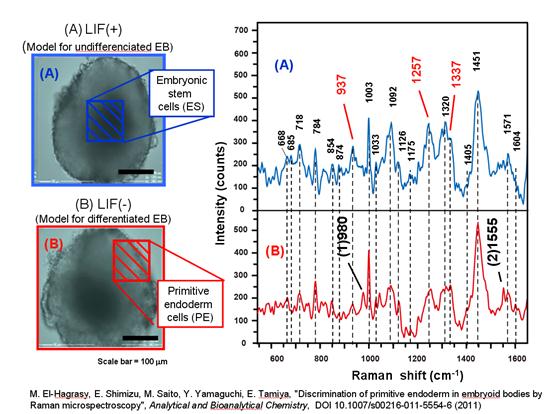 細胞の分化過程を生化学的に理解することは創薬、再生医療におけるの本質的な研究課題である。最終分化後の組織、器官の再生を考慮すると非侵襲であることが望ましい。民谷研究室では、ラマン散乱の方法を利用することにとって、ES細胞(EmbryonicStemCell)の分化過程についてラマン散乱振動モードによる官能基の推定・定性評価および強度による定量評価を行っている。
これまでに、マウスのES細胞について、ES細胞から、胚体細胞塊(EmbryonicBody;EB)、原始胚葉細胞塊
(Primitive Endoderm;PE)に至るまでの分化過程において、ラマン散乱バンドの変化に優位な差があることを見出した。
(図はES細胞塊(A)とPE細胞塊(B)のラマン散乱スペクトルである)
細胞の分化過程を生化学的に理解することは創薬、再生医療におけるの本質的な研究課題である。最終分化後の組織、器官の再生を考慮すると非侵襲であることが望ましい。民谷研究室では、ラマン散乱の方法を利用することにとって、ES細胞(EmbryonicStemCell)の分化過程についてラマン散乱振動モードによる官能基の推定・定性評価および強度による定量評価を行っている。
これまでに、マウスのES細胞について、ES細胞から、胚体細胞塊(EmbryonicBody;EB)、原始胚葉細胞塊
(Primitive Endoderm;PE)に至るまでの分化過程において、ラマン散乱バンドの変化に優位な差があることを見出した。
(図はES細胞塊(A)とPE細胞塊(B)のラマン散乱スペクトルである)
(4)プリンタブル電気化学バイオセンサーに関する研究
高性能プリンタブル電極の開発
POCT指向型バイオセンサーの開発
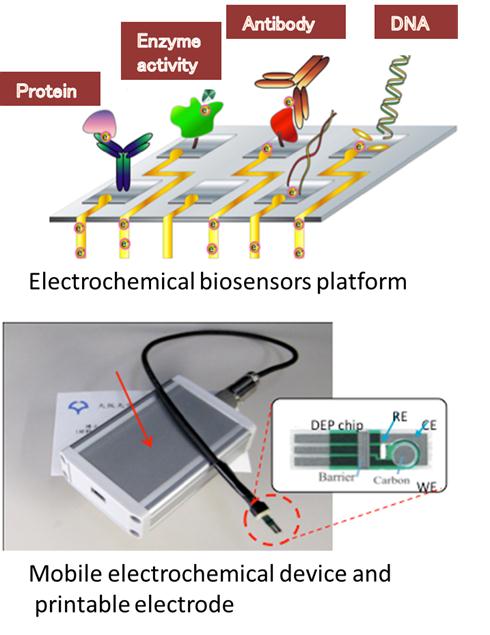 遺伝子、タンパク、細胞シグナルなどのバイオマーカーを電極反応を用いて評価する電気化学バイオセンサー研究を行っている。特に、プリンタブル電極は、量産可能でディスポーザブルであるため、健康医療診断、食品安全性検査などにきわめて有用である。すでに、これを用いて簡便型遺伝子診断を実現し、サルモネラやO-157大腸菌などの食中毒菌、インフルエンザウイルス、遺伝子組み換え食品、肉質判定(ハラル診断など)などに成功している。遺伝子センサー以外にも金ナノ粒子―抗体を用いたイムノセンサー、酸化還元マーカーを用いた食品の抗酸化能評価、残留農薬検出などへの応用も進めている。さらに、小型軽量な電気化学測定装置を開発し、現場での測定を可能とするPOCT(Point of care testing) を指向したバイオセンサー開発を進めている。
遺伝子、タンパク、細胞シグナルなどのバイオマーカーを電極反応を用いて評価する電気化学バイオセンサー研究を行っている。特に、プリンタブル電極は、量産可能でディスポーザブルであるため、健康医療診断、食品安全性検査などにきわめて有用である。すでに、これを用いて簡便型遺伝子診断を実現し、サルモネラやO-157大腸菌などの食中毒菌、インフルエンザウイルス、遺伝子組み換え食品、肉質判定(ハラル診断など)などに成功している。遺伝子センサー以外にも金ナノ粒子―抗体を用いたイムノセンサー、酸化還元マーカーを用いた食品の抗酸化能評価、残留農薬検出などへの応用も進めている。さらに、小型軽量な電気化学測定装置を開発し、現場での測定を可能とするPOCT(Point of care testing) を指向したバイオセンサー開発を進めている。
References:1) Analyst(2011)136,2064, 2) Electroanalysis(2008)20(1)14, 3) Bioelectrochemistry (2008)74(1),118-123, 4) Food Control(2007)18(8)914, 5) Food Control(2010) 21(5) 599-605, 6) Analyst(2009) 134,966
(5)ナノマテリアルを活用したバイオマス燃料電池の研究
ナノ機能電極とバイオエタノール燃料電池
バイオミメチック機能素子の設計
バイオ水素リアクター燃料電池システム
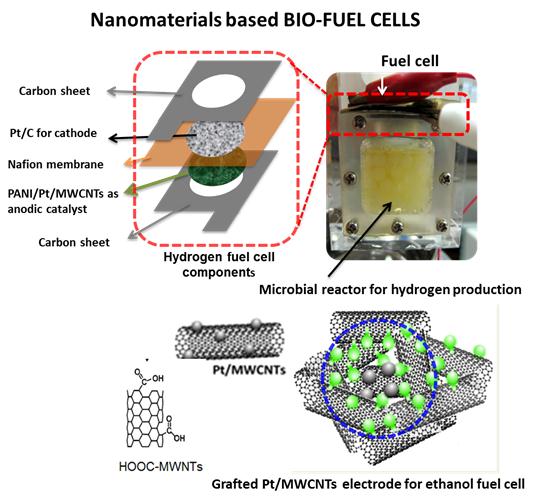 再生可能なエネルギー資源であるバイオマスを原料として直接電気エネルギーへと変換する燃料電池の研究を行っている。特に、導電性ポリマー、カーボンナノチューブ(CNT)、金属ナノ粒子などを用いた燃料電池電極の活性の向上を検討している。たとえば、導電性ポリマーであるポリアニリンをCNT上に電解重合にて形成させることにより水素に対して約6倍の出力向上を実現し、これに水素生産微生物リアクターと直接連結したシステムを開発した。また、微生物反応で得られるエタノールを濃縮せずに電気エネルギーに変換するために、燃料電池のアノード電極に白金ナノ粒子を形成させたCNTにポリアニリンやポリピロールを電解重合したり、CNTにカルボキシル基を導入し電極上で微小な凝集構造を形成させることにより、高い電流密度を得ることも実現している。また、セルロースといったバイオポリマーやグルコース以外の各種単糖類からの直接電気エネルギー変換と物質変換も試みている。その他、CNTに官能基を導入することにより、多糖類の加水分解するBio-inspired catalystの設計も進めている。
再生可能なエネルギー資源であるバイオマスを原料として直接電気エネルギーへと変換する燃料電池の研究を行っている。特に、導電性ポリマー、カーボンナノチューブ(CNT)、金属ナノ粒子などを用いた燃料電池電極の活性の向上を検討している。たとえば、導電性ポリマーであるポリアニリンをCNT上に電解重合にて形成させることにより水素に対して約6倍の出力向上を実現し、これに水素生産微生物リアクターと直接連結したシステムを開発した。また、微生物反応で得られるエタノールを濃縮せずに電気エネルギーに変換するために、燃料電池のアノード電極に白金ナノ粒子を形成させたCNTにポリアニリンやポリピロールを電解重合したり、CNTにカルボキシル基を導入し電極上で微小な凝集構造を形成させることにより、高い電流密度を得ることも実現している。また、セルロースといったバイオポリマーやグルコース以外の各種単糖類からの直接電気エネルギー変換と物質変換も試みている。その他、CNTに官能基を導入することにより、多糖類の加水分解するBio-inspired catalystの設計も進めている。
References: 1) Biosens. Bioelectron 25, 2509(2010) J. Mater. Chem. 21, 4068 (2011), 2) Electrochem. Commun. 13, 746 (2011), 3) Electrochim. Acta, 56, 9875 (2011), 4) Chem. Commun., 47, 7176-7178 (2011), 5) Biosens. and Bioelectron., 30, 204-210 (2011)